
| student study |
| of school |
| A.Na+ | B.二氧化碳 | C.RNA | D.胰岛素 |
2.哺乳动物肝细胞的代谢活动十分旺盛,下列细胞结构与对应功能表述有误的是
A.细胞核:遗传物质储存与基因转录 B.线粒体:丙酮酸氧化与 ATP合成C.高尔基体:分泌蛋白合成与加工D.溶酶体:降解失去功能细胞组分
3.光反应在叶绿体类囊体上进行,适宜条件下,向类囊体悬液中加入氧化还原指示剂DCIP,照光后 DCIP由蓝色变为无色,反应过程中
| A.需要 ATP 提供能量 | B.DCIP 被氧化 | C.不需要光合色素参与 | D.会产生氧气 |
4.以下高中生物学实验中,操作不正确的是
A.在制作果酒的实验中,将葡萄汁液装满整个发酵装置 B.鉴定 DNA 时,将粗提产物与二苯胺混合后进行沸水浴
C.用苏丹Ⅲ染液染色,观察花生子叶细胞中的脂肪滴(颗粒) D.用龙胆紫染液染色,观察洋葱根尖分生区细胞中的染色体
5.用 Xho I 和 Sal I 两种限制性核酸内切酶分别处理同一 DNA 片段,酶切位点及酶切产物分离结果如图。以下叙述不正确的是
A.图1中两种酶识别的核苷酸序列不同 B.图2中酶切产物可用于构建重组 DNA
C.泳道①中是用 Sal I处理得到的酶切产物 D.图中被酶切的 DNA 片段是单链 DNA![]()
6.下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
7.科研人员提出由 CO2 和 CH4 转化为高附加值产品 CH3COOH 的催化反应历程。历程示意图如下。 说法不正确的是:
A.生成 CH3COOH 总反应的原子利用率为100% B.Ch4→CH3COOH 过程中,有 C-H 键发生断裂
C.①→②放出能量并形成了 C一C 键 D.该催化剂可有效提高反应物的平衡转化率
8.化学用语对事实的表述不正确是 A.硬脂酸与乙醇的酯化反应:C17H35COOH + C2H518OH ![]() C17H35COOC2H5 + H218O
C17H35COOC2H5 + H218O
B.常温时,0.1 mol·L−1 氨水的 pH = 11.1:NH3·H2O![]() NH
NH![]() + OH−
+ OH−
C.由 Na 和 C1 形成离子键的过程: Nax + Cl → Na+[ Cl ]−Na D.电解精炼铜的阴极反应:Cu2+ + 2e− = Cu
9.下列实验中的颜色变化,与氧化还原反应无关的是
A. NaOH 溶液滴入 FeSO4 溶液中;产生白色沉淀,随后变为红褐色。B.石蕊溶液滴入氯水中;溶液变红,随后迅速褪色。
C. Na2S 溶液滴入 AgCl 浊液中;沉淀由白色逐渐变为黑色。D.热铜丝插入稀硝酸中;产生无色气体,随后变为红棕色。
10.一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。其结构片段如下图 。下列关于该高分子的说法正确的是
A.完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境 B.完全水解产物的单个分子中,含有官能团—COOH 或—NH2
C.氢键对该高分子的性能没有影响 D.结构简式为:
11.测定0.1 mol·L−1 Na2SO3 溶液先升温再降温过程中的 pH,数据如下。 温度25℃-PH9.66。温度30℃-PH9.52。温度40℃-PH9.37。温度25℃-PH9.25。实验过程中,取①④时刻的溶液,加入盐酸酸化的 BaCl2 溶液做对比实验,④产生白色沉淀多。下列说法不正确的是
A.Na2SO3 溶液中存在水解平衡:SO![]() + H2O
+ H2O ![]() HSO
HSO![]() + OH− B.④的 pH 与①不同,是由于SO
+ OH− B.④的 pH 与①不同,是由于SO![]() 浓度减小造成的
浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致 D.①与④的 Kw 值相等
12.验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3% NaCl 溶液)。 下列说法不正确的是
① 溶液中Zn棒Fe棒,Fe 表面生成蓝色沉淀;②溶液中Zn棒Fe棒,一段时间无明显变化;③溶液中Fe棒,一段时间试管内生成蓝色沉淀
| A.对比②③,可以判定 Zn 保护了 Fe | B.对比①②, K3[Fe(CN)6]可能将 Fe 氧化 | |
| C.验证 Zn 保护 Fe 时不能用①的方法 | D.将 Zn 换成 Cu,用①的方法可判断 Fe 比 Cu 活泼 |
13.在核反应方程中 ![]() He + N → O + X ,X 表示的是 A.质子 B.中子 C.电子 D.a粒子
He + N → O + X ,X 表示的是 A.质子 B.中子 C.电子 D.a粒子
14.关于分子动理论,下列说法正确的是 A.气体扩散的快慢与温度无关
B.布朗运动是液体分子的无规则运动 C.分子间同时存在着引力和斥力D.分子间的引力总是随分子间距增大而增大
15.用双缝干涉实验装置得到白光的干涉条纹,在光源与单缝之间加上红色滤光片后
| A.干涉条纹消失 | B.彩色条纹中的红色条纹消失 | C.中央条纹变成暗条纹 | D.中央条纹变成红色 |
16.如图所示,一列简谐横波向右传播,P、Q 两质点平衡位置相距0.15m。当 P 运动到上方最大位移处时,Q 刚好运动到下方最大位移处,则这列波的波长可能是A.0.60m B.0.30m C.0.20m D.0.15m
17.若想检验"使月球绕地球运动的力"与"使苹果落地的力"遵循同样的规律,在已知月地距离约为地球半径60倍的情况下,需要验证
| A.地球吸引月球的力约为地球吸引苹果的力的 1/602 | B.月球公转的加速度约为苹果落向地面加速度的 1/602 | |
| C.自由落体在月球表面的加速度约为地球表面的 1/6 | D.苹果在月球表面受到的引力约为在地球表面的 1/60 |
18.某空间存在匀强磁场和匀强电场。一个带电粒子(不计重力)以一定初速度射入该空间后,做匀速直线运动;若仅撤除电场,则该粒子做匀速圆周运动,下列因素与完成上述两类运动无关的是A.磁场和电场的方向B.磁场和电场的强弱C.粒子的电性和电量D.粒子入射时的速度
19.研究与平行板电容器电容有关因素的实验装置如图所示,下列说法正确的是 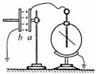
A.实验前,只用带电玻璃棒与电容器 a 板接触,能使电容器带电
B.实验中,只将电容器 b 板向上平移,静电计指针的张角变小
C.实验中,只在极板间插入有机玻璃板,静电计指针的张角变大
D.实验中,只增加极板带电量,静电计指针的张角变大,表明电容增大
20.根据高中所学知识可知,做自由落体运动的小球,将落在正下方位置。但实际上,赤道上方200m 处无初速下落的小球将落在正下方位置偏东约6cm 处,这一现象可解释为,除重力外,由于地球自转,下落过程小球还受到一个水平向东的"力",该"力"与竖直方向的速度大小成正比,现将小球从赤道地面竖直上抛,考虑对称性,上升过程该"力"水平向西,则小球 A.到最高点时,水平方向的加速度和速度均为零
B.到最高点时,水平方向的加速度和速度均不为零C.落地点在抛出点东侧 D.落地点在抛出点西侧
第二部分(非选择题 共180分)本部分共11小题,共180分。
21.(18分)用图1所示的实验装置研究小车速度随时间变化的规律。主要实验步骤如下:![]()
a.安装好实验器材。接通电源后,让拖着纸带的小车沿长木板运动,重复几次。
b.选一条纸带,找个点当作计时起点 O(t = 0),每隔相同的时间间隔 T 选取一个计数点,如图2中A、B、C、D、E、F……所示。
c.通过测量、计算可以得到在打 A、B、C、D、E……点时小车的速度,分别记作v1、v2、v3、v4、v5……
d.以速度 v 为纵轴、时间 t 为横轴建立直角坐系,在坐标纸上描点,如图3所示
结合上述实验步骤,请你完成下列任务:
(1)在下列仪器和器材中,还需要使用的_____和_____(填选项前的字母)。
A.电压合适的50Hz 交流电源B.电压可调的直流电C.刻度尺D.秒表E.天平(含砝码)
(2)在图3中已标出计数点 A、B、D、E 对应的坐标点,请在该图中标出计数点 C 对应的坐标点,并画出 v-t 图像。
(3)观察 v-t 图像,可以判断小车做匀变速直线运动,其依据是______。v-t 图像斜率的物理意义是______。
(4)描绘 v-t 图像前,还不知道小车是否做匀变速直线运动。用平均速度 ∆x/∆t 表示各计数点的瞬时速度,从理论上讲,对 ∆t 的要求是_____(选填"越小越好"或"与大小无关");从实验的角度看,选取的 ∆x 大小与速度测量的误差____(填有关或无关)。
(5)早在16世纪末,伽利略就猜想落体运动的速度应该是均匀变化的。当时只能靠滴水计时,为此他设计了如图4所示的"斜面实验",反复做了上百次,验证了他的猜想。请你结合匀变速直线运动的知识,分析说明如何利用伽利略"斜面实验"检验小球的速度是随时间均匀变化的。
22.(16分)2022年将在我国举办第二十四届冬奥会,跳台滑雪是其中最具观赏性的项目之一。某滑道示意图如下,长直助滑道 AB 与弯曲滑道BC 平滑衔接,滑道 BC 高 h = 10m ,C是半径R = 20m圆弧的最低点,质量m = 60kg的运动员从 A 处由静止开始匀加速下滑,加速度a= 4.5m/s2,到达 B 点时速度 vB = 30m/s 。取重力加速度 g = 10m/s2。 (1)求长直助滑道 AB 的长度 L ;
(2)求运动员在 AB 段所受合外力冲量的 I 大小 ; (3)若不计 BC 段阻力,画出运动员经C 点时受力图,求其所受支持力 FN 大小。
23.(18分)如图1所示,用电动势为 E、内阻为 r 的电源,向滑动变阻器 R 供电。改变变阻器 R 的阻值,路端电压 U 与电流 I 均随之变化。
(1)以 U 为纵坐标,I 为横坐标,在图2中画出变阻器阻值 R 变化过程中 U-I 图像的示意图,并说明 U-I 图像与两坐标轴交点的物理意义。
(2)a.请在图2画好的 U-I 关系图线上任取一点,画出带网格的图形,以其面积表示此时电源的输出功率;
b.请推导该电源对外电路能够输出的最大电功率及条件。
(3)请写出电源电动势定义式,并结合能量守恒定律证明:电源电动势在数值上等于内、外电路电势降落之和。 
24.(20分)(1)静电场可以用电场线和等势面形象描述。
a.请根据电场强度的定义和库仑定律推导出点电荷 Q 的场强表达式;
b.点电荷的电场线和等势面分布如图所示,等势面 S1、S2 到点电荷的距离分别为 r1、r2。我们知道,电场线的疏密反映了空间区域电场强度的大小。请计算 S1、S2 上单位面积通过的电场线条数之比 N1/N2。
(2)观测宇宙中辐射电磁波的天体,距离越远单位面积接收的电磁波功率越小,观测越困难。为了收集足够强的来自天体的电磁波,
增大望远镜口径是提高天文观测能力的一条重要路径。2016年9月25日,世界上最大的单口径球面射电望远镜 FAST 在我国贵州
落成启用,被誉为"中国天眼"。FAST 直径为500m,有效提高了人类观测宇宙的精度和范围。
a. 设直径为100m 的望远镜能够接收到的来自某天体的电磁波功率为 P1,计算 FAST 能够接收到的来自该天体的电磁波功率P2;
b. 在宇宙大尺度上,天体的空间分布是均匀的,仅以辐射功率为 P 的同类天体为观测对象,设直径为100m 望远镜能够观测到的
此类天体数目是 N0,计算 FAST 能够观测到的此类天体数目 N。
25.(17分)8-羟基喹啉被广泛用作金属离子的洛合剂和萃取剂,也是重要的医药中间体。下图是8-羟基喹啉的合成路线。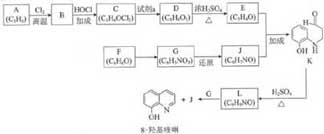
已知:ⅰ.![]()
ⅱ.同一个碳原子上连有2个羟基的分子不稳定。
(1)按官能团分类,A 的类别是_______。 (2)A→B 的化学方程式是:______。
(3)C 可能的结构简式是_____。 (4)C→D 所需的试剂 a 是________。
(5)D→E 的化学方程式是_______。 (6)F→G的反应类型是________。
(7)将下列 K→L 的流程图补充完整:
(8)合成8-羟基喹啉时,L 发生了______(填氧化或还原)反应,反应时还生成了水,则 L 与 G 物质的量之比为______。
26.(13分)磷精矿湿法制备磷酸的一种工艺流程如下:![]()
已知:磷精矿主要成分为 Ca5(PO4)3(OH),还含有 Ca5(PO4)3F 和有机碳等。
溶解度:Ca5(PO4)3(OH) < CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有_____。
(2)磷精矿粉酸浸时发生反应: 2Ca5(PO4)3(OH) + 3H2O + 10H2SO4 =10CaSO4·0.5H2O + 6H3PO4
①该反应体现出酸性关系: H3PO4_____H2SO4(填>或< )。 ②结合元素周期律解释①中结论: P 和 S 电子层数相同,_________。
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:________。
(4)H2O2 将粗磷酸中的有机碳氧化为 CO2 脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:______。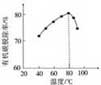
(5)脱硫时,CaCO3 稍过量,充分反应后仍有SO![]() 残留,原因是:________;加入BaCO3可进一步提高硫的脱除率,其离子方程式是_____。
残留,原因是:________;加入BaCO3可进一步提高硫的脱除率,其离子方程式是_____。
(6)取 a g 所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用 b mol·L−1 NaOH 溶液滴定至终点时生成Na2HPO4 ,消耗NaOH溶液c mL,精制磷酸中H3PO4的质量分数是______(已知:H3PO4 摩尔质量为98 g·mo−1)。
27.(12分)研究人员用含硫物质热化学循环实现太阳能的转化与存储。过程如下: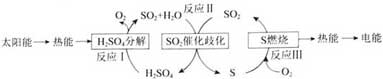
(1)反应Ⅰ: 2H2SO4(1)=2SO2(g)+ 2H2O(g) + O2(g) △H1= +551 KJ·mol−1
反应Ⅲ:S(s) + O2(g) = SO2(g) △H3= -297 KJ·mol−1
反应Ⅱ的热化学方程式:______。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4 在平衡体系中物质的量分数随温度的变化关系如图所示。P2___P1 (填>或<),得出该结论的理由是________。
(3)I− 可以作为水溶液中SO2 歧化反应的催化剂,可能的催化过程如下。将 ii 补充完整。
i.SO2 + 4I− + 4H+ = S↓+ 2I2 + 2H2O ii.I2 + 2H2O +______ =_______ +_______ + 2I−
(4)探究 i、ii 反应速率与 SO2 歧化反应速率的关系,实验如下:分别将18mL SO2 饱和溶液加入到2mL 下列试剂中,密闭放置观察现象。(已知:I2 易溶解在 KI 溶液中)
A.0.4 mol·L−1 KI;溶液变黄,一段时间后出现浑浊。 B.a mol·L−1 KI,0.2 mol·L−1 H2SO4;溶液变黄,出现浑浊较 A 快。
C.0.2 mol·L−1,H2SO4;无明显现象。 D.0.2 mol·L−1 KI,0.0002 mol I2;溶液由棕褐色很快褪色,变成黄色,出现浑浊较 A 快。
①B 是 A 的对比实验,则 a =_______。 ②比较 A、B、C,可得出的结论是_______。
③实验表明,SO2 的歧化反应速率 D > A,结合 i、ii 反应速率解释原因:_______。
28.(16分)实验小组制备高铁酸钾( K2FeO4 )并探究其性质。
资料: K2FeO4 为紫色固体,微溶于 KOH 溶液:具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备 K2FeO4 (夹持装置略) 浓盐酸和KMnO4
①A 为氯气发生装置。A 中反应方程式是________(锰被还原为 Mn2+)。 ②将除杂装置 B 补充完整并标明所用试剂。
③C 中得到紫色固体和溶液。C 中 Cl2 发生的反应有3Cl2 + 2Fe(OH)3 + 10KOH = 2K2FeO4 + 6KCl + 8H2O ,另外还有______。
(2)探究 K2FeO4 的性质。
①取 C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a ,经检验气体中含有Cl2 ,为证明是否K2FeO4氧化了Cl− 而产生Cl2 ,设计以下方案:
方案Ⅰ: 取少量 a,滴加 KSCN 溶液至过量,溶液呈红色。
方案Ⅱ: 用KOH 溶液充分洗涤C中所得固体,再用KOH 溶液将K2FeO4 溶出,得到紫色溶液b ,取少量 b ,滴加盐酸,有Cl2 产生。
ⅰ.由方案Ⅰ中溶液变红可知a 中含有__离子,但该离子的产生不能判断一定是K2FeO4 将Cl− 氧化,还可能由__产生(用方程式表示)。
ⅱ.方案Ⅱ可证明 K2FeO4 氧化了 Cl− ,用 KOH 溶液洗涤的目的是__________。
②根据 K2FeO4的制备实验得出:氧化性Cl2___FeO![]() (填">"或"< "),而方案Ⅱ实验表明,Cl2 和 FeO
(填">"或"< "),而方案Ⅱ实验表明,Cl2 和 FeO![]() 的氧化性强弱关系相反,原因是___。
的氧化性强弱关系相反,原因是___。
③资料表明,酸性溶液中的氧化性 FeO![]() > MnO
> MnO![]() ,验证实验如下:将溶液 b 滴入 MnSO4 和足量 H2SO4 的混合溶液中,振荡后溶液呈浅紫色。该现象能否证明氧化性 FeO
,验证实验如下:将溶液 b 滴入 MnSO4 和足量 H2SO4 的混合溶液中,振荡后溶液呈浅紫色。该现象能否证明氧化性 FeO![]() > MnO
> MnO![]() ,若能,请说明理由;若不能,进一步设计实验方案。理由或方案: _________。
,若能,请说明理由;若不能,进一步设计实验方案。理由或方案: _________。
29.(17分)研究人员利用与癌细胞在某些方面具有相似性的诱导多能干细胞(iPSC)进行了抗肿瘤的免疫学研究.
(1)癌细胞具有无限_______的特点。当体内出现癌细胞时,可激发机体的________系统发挥清除作用。
(2)研究人员进行的系列实验如下:
免疫组小鼠:每周注射1次含失去增殖活性的 iPSC 悬液,连续4周; 空白组小鼠:每周注射1次不含失去增殖活性的 iPSC 缓冲液,连续4周。
实验一:取免疫组和空白组小鼠的血清分别与 iPSC、DB7(一种癌细胞)和MEF(一种正常体细胞)混合,检测三种细胞与血清中抗体的结合率。
免疫组: iPSC-77;DB7-82;MEF-8。空白组:iPSC-10;DB7-8;MEF-9。
①比较表中 iPSC 与两组小鼠血清作用的结果可知,免疫组的数值明显_____空白组的数值,说明 iPSC 刺激小鼠产生了特异性抗体。
②表中 DB7和 iPSC 与免疫组小鼠血清作用后的检测数据无明显差异,说明 DB7有_________。
③综合表中全部数据,实验结果表明_______。
实验二:给免疫组和空白组小鼠皮下注射 DB7,一周后皮下形成肿瘤。随后空白组小鼠肿瘤体积逐渐增大,免疫组小鼠肿瘤体积逐渐缩小。由此推测:iPSC 还能刺激机体产生特异性抗肿瘤的_________免疫。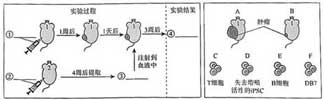
(3)研究人员另取小鼠进行实验,验证了上述推测。下图为实验组的实验过程及结果示意图。请在下图中选择 A 或 B 填入④处,从 C~F 中选择字母填入①~③处。
(4)该系列研究潜在的应用前景是 iPSC 可以用于_______。
30.(17分)稻瘟病是由稻瘟病菌(Mp)侵染水稻引起的病害,严重危害我国粮食生产安全。与使用农药相比,抗稻瘟病基因的利用是控制稻瘟病更加有效、安全和经济的措施。
(1)水稻对Mp表现出的抗病与感病为一对相对________,为判断某抗病水稻是否为纯合子,可通过观察自交子代_____来确定。
(2)现有甲(R1R1r2r2r3r3)、乙(r1r1R2R2r3r3)、丙(r1r1r2r2R3R3)三个水稻抗病品种。抗病(R)对感病(r)为显性,三对抗病基因位于不同染色体上。根据基因的 DNA 序列设计特异性引物,用 PCR 方法可将样本中的 R1、r1、R2、r2、R3、r3 区分开。这种方法可用于抗病品种选育中基因型的鉴定。
①甲品种与感病品种杂交后,对F2 不同植株的R1、r1进行PCR扩增。已知R1比 r1片段短。从扩增结果(下图)推测可抗病的植株有与___。
M:标准 DNA 片段。1:植株1。2:植株2。3:植株3。
②为在短时间内将甲、乙、丙三重品种中的抗病基因整合,选育新的纯合抗病植株,下列育种步骤的正确排序是___。
a.甲×乙,得到 F1 b.用 PCR 方法选出 R1R1R2R2R3R3 植株
c.R1r1R2r2r3r3 植株×丙,得到不同基因型的子代 d.用 PCR 方法选出 R1r1R2r2R3r3 植株,然后自交得到不同基因型的子代
(3)研究发现,水稻的抗病表现不仅需要自身抗病基因(R1、R2、R3等)编码的蛋白,也需要 Mp 基因(A1、A2、A3等)编码的蛋白。只有 R 蛋白与相应的 A 蛋白结合,抗病反应才能被激活。若基因型为 R1R1r2r2R3R3 和 r1r1R2R2R3R3 的水稻,被基因型为
a1a1A2A2a3a3 的 Mp 侵染,推测这两种水稻的抗病性表现依次为_______。
(4)研究人员每年用 Mp(A1A1a2a2a3a3)人工接种水稻品种甲(R1R1r2r2r3r3),几年后甲品种丧失了抗病性,检测水稻的基因未发现变异。推测甲品种抗病性丧失的原因是_______。
(5)水稻种植区的 Mp 是由不同基因型组成的群体。大面积连续种植某个含单一抗病基因的水稻品种,将会引起 Mp 种群______,使该品种抗病性逐渐减弱直至丧失,无法在生产中继续使用。
(6)根据本题所述水稻与 Mp 的关系,为避免水稻品种抗病性丧失过快,请从种植和育种两个方面给出建议_______。
31.(16分)因含 N、P 元素的污染物大量流入,我国某大型水库曾连续爆发"水华"。为防治"水华",在控制上游污染源的同时,研究人员依据生态学原理尝试在水库中投放以藻类和浮游动物为食的鲢鱼和鱅鱼,对该水库生态系统进行修复,取得了明显效果。
(1)在该水库生态系统组成中,引起"水华"的藻类属于_____。水库中各种生物共同构成_______。
(2)为确定鲢、鳙的投放量,应根据食物网中的营养级,调查投放区鲢、鱸_____的生物积累量(在本题中指
单位面积中生物的总量,以t·hm−2 表示):为保证鲢、鳙的成活率,应捕杀鲢、鱅的_________。
(3)藻类吸收利用水体中的 N、P 元素,浮游动物以藻类为食,银鱼主要以浮游动物为食。由右
图可知,将鲢、鱅鱼苗以一定比例投放到该水库后,造成银鱼生物积累量_____,引起该变化的原因是____。
(4)投放鲢、鳙这一方法是通过人为干预,调整了该生态系统食物网中相关物种生物积累量的___,从而达到改善水质的目的。
(5)鲢鱼和鱅鱼是人们日常食用的鱼类,为继续将投放鲢、鳙的方法综合应用,在保持良好水质的同时增加渔业产量,以实现生态效益和经济效益的双赢,请提出两条具体措施_________。